Ikatan Ionik
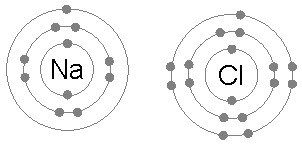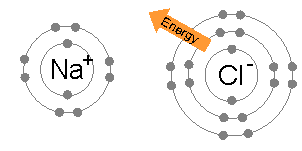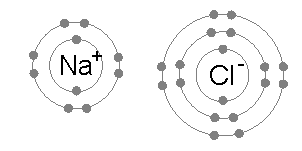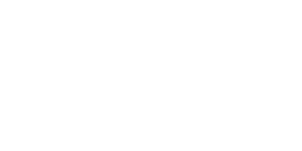
Suatu logam dikatakan stabil, jika atom tersebut mempunyai konfigurasi elektron
seperti konfigurasi elektron pada gas mulia yaitu terdapat delapan elektron
pada skell tea lower (dua elektron bila atom mempunyai hanya satu skell). Jika
suatu atom hanya memilki satu elektron pada skell teabar maka ia cenderung
melepas elektron tersebut. Dan skell yang lebih ke dalam yang perlakuaannya
sudah penuh akan menjadi skell tealoar. Hal ini yang menyebabkan suatu atom
menjadi lebih satabil tetapi hal ini juga menyebabkan atom itu kelebihan atom
proton (yang bermuatan positif) sehingga atom tersebut akan bermuatan positif
dan atom tersebut berubah menjadi ion positif. Sebaliknya bila suatu atom yang
memiliki tujuh elektron skell terluarnya maka akan cenderung menerima satu
elektron lagi dari luar. Jika hal ini terjadi maka atom tersebut akan bermuatan
negatif (karena kelebihan elektron).
Jika kedua atom ini berdekatan maka akan terjadi tarik-menarik karena
kedua ion tersebut memiliki muatan listrik yang berlawanan. Ikatan ini disebut
juga dengan ikatan ion.
Ikatan Kovalen

Beberapa atom dapat memperoleh konfigurasi elektron yang
stabil dengan saling meminjamkan elektronnya. Dengan saling meminjamkan
elektron dari atom, atom akan memperoleh susunan elektron yang stabil tanpa
menyebabkan menjadi bermuatan. Ikatan atom terjadi melalui elektron yang saling
dipinjamkan itu. Elektron ini masih memiliki ikatan atom aslinya, tetapi juga
sudah terikat atom yang meminjamnya.
Ikatan Logam
Dalam atom juga terjadi saling meminjamkan elektron, hanya
saja jumlah atom yang bersama-sama saling meminjamkan elektron valensinya
(elektron berada pada skell tealoar) itu tidak hanya antara 2 atom tetapi dalam
beberapa atom dalam jumlah yang tak terbatas. Setiap atom menyerahkan elektron
valensinya untuk digunakan bersama. Dengan demikian akan ada ikatan
tarik-menarik antara atom-atom yang saling berdekatan. Jarak antar atom ini
akan tetap (kondisi yang sama). Bila ada atom yang bergerak menjauh maka gaya
tarik-menarik akan menariknya kembali seperti semula dan bila bergerak terlalu
mendekat maka akan timbul gaya tolak-menolak karena atom bergerak terlalu dekat
padahal muatan listriknya sama, sehingga kedudukan atom relatif terhadap atom
lain akan tetap. Ikatan seperti ini dinamakan ikatan logam. Pada ikatan ini
inti-inti atom terletak beraturan dengan jarak tertentu sedangkan elektron yang
dipinjamkan seolah-olah membentuk “kabut elektron” yang mengisi sela-sela inti.




0 Komentar
Terima Kasih Atas Kunjungan & Komentar Anda di Agung Blog